肥胖症研究相关因子之白细胞介素31(IL-31)
全球肥胖症流行率持续攀升,已成为引发2型糖尿病、心血管疾病、非酒精性脂肪肝等多种代谢并发症的核心危险因素。其病理机制复杂,涉及脂肪组织重塑、免疫微环境失衡及全身慢性低度炎症的协同作用。
IL-31是IL-6超家族成员之一,是一种具有多重生物学功能的分泌性糖蛋白,IL-31由164个氨基酸组成,分子量约为18.2 kDa,其编码基因定位于染色体12q24.31,通过选择性剪接可产生多种亚型,不同亚型的生物活性存在细微差异,但核心功能均围绕炎症调控与代谢调节展开。IL-31的信号传导依赖于异二聚体受体复合物,该复合物由特异性亚基IL-31RA(IL-31受体α)与共享亚基OSMRβ(抑瘤素M受体β)组成,这两种受体广泛表达于脂肪细胞、免疫细胞(巨噬细胞、T淋巴细胞、树突状细胞等)、上皮细胞及中枢神经系统神经元,为IL-31多靶点调控提供了结构基础。
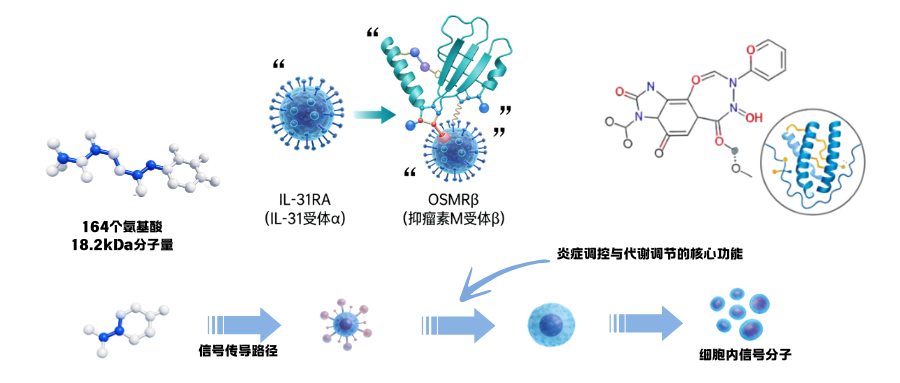
IL-31主要由活化的免疫细胞和结构细胞分泌。正常生理状态下,IL-31表达水平较低,主要由Th2细胞、巨噬细胞、肥大细胞等免疫细胞少量分泌,参与机体免疫稳态调节;而在肥胖状态下,脂肪组织成为IL-31的主要分泌来源——肥大的脂肪细胞可直接合成并分泌IL-31,同时,浸润至脂肪组织的巨噬细胞、Th2细胞等免疫细胞,在局部炎症微环境的刺激下,会大量释放IL-31,导致血清及脂肪组织中IL-31水平显著升高。
生理功能
IL-31通过结合其特异性受体复合物,激活JAK-STAT、MAPK、PI3K-AKT等下游信号通路,发挥促炎、免疫调节、代谢调控及神经刺激等多重生理功能,这些功能在肥胖状态下发生病理性异常,成为驱动肥胖进展及并发症发生的重要机制。
1.强力介导慢性炎症反应
IL-31是慢性炎症反应的核心驱动因子,可特异性诱导Th2型免疫反应,促进IL-4、IL-5、IL-13等细胞因子释放,并激活巨噬细胞与T淋巴细胞的浸润及活化,进而刺激TNF-α、IL-6、CCL17/22等促炎因子分泌,形成“IL-31-促炎因子”的正反馈放大环路。同时,IL-31抑制IL-10、脂联素等抗炎因子表达,打破炎症平衡,加剧慢性低度炎症状态。
2.调控脂肪组织代谢与分化
IL-31直接参与脂肪代谢调控:一方面激活前脂肪细胞向成熟脂肪细胞分化,加速脂质合成与储存,促进脂肪堆积;另一方面抑制脂肪细胞脂解作用,减少游离脂肪酸氧化分解,降低能量消耗,形成“易胖”代谢表型。此外,它还干扰棕色/米色脂肪的产热功能,进一步降低能量代谢效率,加重脂肪过度蓄积。
3.诱导胰岛素抵抗发生
IL-31是诱发胰岛素抵抗的关键因子,可直接抑制胰岛素信号通路中的IRS-1/PI3K-Akt关键分子,降低脂肪细胞、肝细胞及骨骼肌细胞对胰岛素的敏感性。同时,它通过介导慢性炎症损害胰岛β细胞功能,减少胰岛素分泌,并促进肝糖异生、抑制外周组织糖利用,最终诱发高血糖,推动肥胖向2型糖尿病进展。
4.介导神经-免疫-代谢交互作用
IL-31是连接神经、免疫与代谢系统的关键分子:作用于中枢神经系统的感觉神经元时,可引发顽固性瘙痒,解释了肥胖患者常见的皮肤病变;干扰中枢瘦素、饥饿素的信号传导时,会导致食欲亢进、摄食增加,加重脂肪堆积,形成“肥胖-IL-31升高-食欲亢进-更严重肥胖”的恶性循环;此外,它破坏肠道屏障完整性,诱发肠漏并促进内毒素入血,参与肠-脂肪-脑轴的调控失衡。


 销售咨询
销售咨询